Etiqueta: Biológicos
Biotecnológicos en Colombia: Panorama nacional de reglamentación y acceso
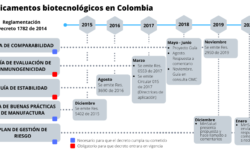
Contexto de los biotecnológicos Como es de conocimiento de quienes siguen los temas de acceso a medicamentos en el mundo, los medicamementos biológicos y biotecnológicos son las tecnologías más recientes y que están transformando el tratamiento de múltiples dolencias y de paso el mercado de los medicamentos global y los…
[COLOMBIA] Consejo de Estado niega medidas cautelares sobre artículo 9 del Decreto 1782 de 2014: una decisión en pro del acceso a medicamentos

Esta semana Colombia recibió una excelente y esperanzadora noticia en materia de acceso a medicamentos, concretamente los medicamentos biotecnológicos, utilizados para enfermedades como cáncer, diabetes y artritis y que son los que tienen mayores ventas en el país. El pasado lunes 29 de abril, el Consejo de Estado emitió su…
OMS y los medicamentos biotecnológicos. Nuestra participación y aportes

En este momento está en curso un importante proceso de decisión al interior de la Organización Mundial de la Salud relacionado con la sostenibilidad de los sistemas de salud, el acceso a medicamentos y el avance de la ciencia. El cuento es así: Los medicamentos biotecnológicos son una creciente fuente…
Participamos en la consulta de la OMS sobre documento técnico de medicamentos biotecnológicos y biosimilares

En febrero de la mano de IFARMA, lideramos la participación del Comité de Veeduría y Cooperación en Salud, acompañados el Centro de Información de Medicamentos de la Universidad Nacional, la Federación Médica Colombiana, el Observatorio del Medicamento de la Federación Médica Colombiana y la Conferencia Episcopal de Colombia, en la…
#Opinión en Contagio Radio y Blogs El Tiempo: Dilema ético para el Consejo de Estado
Biotecnológicos: en Colombia otra vez en riesgo el acceso a medicamentos de calidad y a precio justo

El Decreto 1782 de 2014, que regula la entrada al mercado colombiano de medicamentos biotecnológicos de calidad a precios asquibles, tuvo una larga historia para ser expedido. Culminado este arduo proceso, siguió la emisión de las guías técnicas requeridas para su reglamentación, llegando finalmente a la entrada en vigencia del…
Se corrige Guía de Evaluación de Inmunogenicidad para los medicamentos biológicos

Nos complace informarles que fue publicada la Resolución 0553 de 2017, por la cual el Ministerio de Salud corrige la Guía de Evaluación de Inmunogenicidad para los medicamentos biológicos que había expedido a través de la Resolución 4490 de 2016. De esta manera, ahora si será posible materializar el paso…
Pedimos al Ministerio mantener transparencia en reglamentación de medicamentos biológicos
De la mano con la Fundación IFARMA, radicamos en el despacho del Ministro Alejandro Gaviria un derecho de petición que busca que el proceso de emisión de la Guía de Inmunigenicidad se mantenga en los lineamientos de transparencia y consulta pública que ha caracterizado el proceso general de reglamentación de…
Biotecnológicos en Colombia: Panorama nacional de reglamentación y acceso

Contexto de los biotecnológicos Como es de conocimiento de quienes siguen los temas de acceso a medicamentos en el mundo, los medicamementos biológicos y biotecnológicos son las tecnologías más recientes y que están transformando el tratamiento de múltiples dolencias y de paso el mercado de los medicamentos global y los…
[COLOMBIA] Consejo de Estado niega medidas cautelares sobre artículo 9 del Decreto 1782 de 2014: una decisión en pro del acceso a medicamentos

Esta semana Colombia recibió una excelente y esperanzadora noticia en materia de acceso a medicamentos, concretamente los medicamentos biotecnológicos, utilizados para enfermedades como cáncer, diabetes y artritis y que son los que tienen mayores ventas en el país. El pasado lunes 29 de abril, el Consejo de Estado emitió su…
OMS y los medicamentos biotecnológicos. Nuestra participación y aportes

En este momento está en curso un importante proceso de decisión al interior de la Organización Mundial de la Salud relacionado con la sostenibilidad de los sistemas de salud, el acceso a medicamentos y el avance de la ciencia. El cuento es así: Los medicamentos biotecnológicos son una creciente fuente…
Participamos en la consulta de la OMS sobre documento técnico de medicamentos biotecnológicos y biosimilares

En febrero de la mano de IFARMA, lideramos la participación del Comité de Veeduría y Cooperación en Salud, acompañados el Centro de Información de Medicamentos de la Universidad Nacional, la Federación Médica Colombiana, el Observatorio del Medicamento de la Federación Médica Colombiana y la Conferencia Episcopal de Colombia, en la…
#Opinión en Contagio Radio y Blogs El Tiempo: Dilema ético para el Consejo de Estado
Biotecnológicos: en Colombia otra vez en riesgo el acceso a medicamentos de calidad y a precio justo

El Decreto 1782 de 2014, que regula la entrada al mercado colombiano de medicamentos biotecnológicos de calidad a precios asquibles, tuvo una larga historia para ser expedido. Culminado este arduo proceso, siguió la emisión de las guías técnicas requeridas para su reglamentación, llegando finalmente a la entrada en vigencia del…
Se corrige Guía de Evaluación de Inmunogenicidad para los medicamentos biológicos

Nos complace informarles que fue publicada la Resolución 0553 de 2017, por la cual el Ministerio de Salud corrige la Guía de Evaluación de Inmunogenicidad para los medicamentos biológicos que había expedido a través de la Resolución 4490 de 2016. De esta manera, ahora si será posible materializar el paso…
Pedimos al Ministerio mantener transparencia en reglamentación de medicamentos biológicos
De la mano con la Fundación IFARMA, radicamos en el despacho del Ministro Alejandro Gaviria un derecho de petición que busca que el proceso de emisión de la Guía de Inmunigenicidad se mantenga en los lineamientos de transparencia y consulta pública que ha caracterizado el proceso general de reglamentación de…








