Bogotá. 15 de marzo de 2022
Por Manuel Machado
Subdirector de Misión Salud

Fotografía de: Universidad de Oxford/John Cairns.
Mensajes clave:
- Se cumplieron dos años desde que la Organización Mundial de la Salud (OMS) declaró al Covid-19 como una pandemia. El mundo cambió y la ciencia se vio en una ardua labor investigativa para encontrar curas y tratamientos.
- Los Ensayos Clínicos Controlados son hasta el momento, la mejor herramienta para evaluar eficacia y seguridad de nuevos medicamentos y vacunas, no obstante, algunos eventos adversos no se detectan en dichos ensayos sino en fases de poscomercialización.
- Se deben intensificar los programas de farmacovigilancia en aras de tener la mejor información posible sobre eventos adversos asociados a vacunas incluyendo a aquellos de mayor severidad.
-
Introducción
El 11 de marzo se cumplieron dos años en el que la Organización Mundial de la Salud declaró la pandemia por el Sars-Cov-2 causante del COVID-19. No se tenía idea de lo que se vendría para el mundo y mucho menos para el país. Medidas como cuarentenas, uso del tapabocas obligatorio, comercio restringido, sistemas de salud colapsados y demás, cambiaron el estilo de vida para la población (1).
La ciencia invirtió grandes esfuerzos para encontrar tratamientos y vacunas con el fin de enfrentar la pandemia. A pesar de los cortos tiempos en que se desarrollaron estas vacunas, la evidencia parece ser contundente en términos de eficacia, la cual se traduce en mitigación de síntomas y menores complicaciones de hospitalización y muerte. No obstante, se presentan a continuación algunas reflexiones sobre la seguridad de las mismas a la luz del tiempo transcurrido.
-
Las limitaciones de los Ensayos Clínicos Controlados (ECA)
En las primeras notas elaboradas por Misión Salud a propósito de la pandemia, se mencionaron los riesgos de desarrollar vacunas de forma acelerada. Fueron fabricadas en un periodo de aproximadamente dos años cuando normalmente toma de 10 a 16 años (2).
Leer “El riesgo de aprobar vacunas COVID-19 de manera acelerada”.
Si bien los resultados en términos de eficacia y seguridad de los diversos ECA realizados con vacunas para COVID-19 fueron promisorios, los desenlaces clínicos a largo plazo no están del todo definidos. Es por esta razón que cuando un medicamento o vacuna nueva sale al mercado se debe hacer un seguimiento muy riguroso a potenciales efectos adversos que no se vieron en los ensayos clínicos previos, y en esta situación de pandemia, dicha vigilancia cobra mayor relevancia dada la rapidez con la que se efectuaron dichos ensayos.
Es en este punto donde entra en juego la Farmacovigilancia (FV). Recordando que es definida por la OMS como:
conjunto de actividades para el estudio de la prevención, caracterización, cuantificación y detección de las reacciones adversas asociadas a la medicación (RAM)[1], así como otros problemas asociados a la misma y las consecuencias de su uso en las poblaciones (3,4).
La FV permite ampliar el conocimiento del uso de los medicamentos una vez sean comercializados, identificar eventos adversos que no se detectaron previamente o efectos benéficos no identificados, también facilita a los entes reguladores tomar decisiones sobre el retiro de medicamentos del mercado cuando los riesgos superan los beneficios.
-
Algunos datos de interés de los reportes de FV
Fruto de los programas de FV, se han publicado diferentes reportes sobre los Eventos Adversos Asociados Posteriores a la Vacunación (EAPV). Según el Boletín 09 publicado en enero del presente año, se registraron 35.652 reportes de EAPV de un total de 68.154.006 dosis de vacuna administradas, lo que corresponde a un porcentaje del 0,05% de EAPV. De este último dato, 1.693 eventos corresponden a reacciones graves, sin embargo, no se especifica el tipo ni desenlace de la reacción.
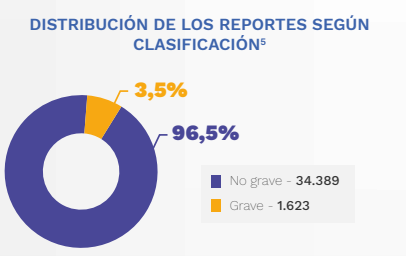
Figura 1. Distribución de reportes de EAPV según gravedad. Tomado de (5).
Aunque dichos informes se han publicado con cierta periodicidad sería deseable que se diera información en detalle de los EAPV. Si bien se han presentado en una baja proporción, es indispensable que se haga una descripción y análisis detallados en aras de dar garantía a los procesos de transparencia, aportar a la evidencia y facilitar la toma de decisiones en salud pública. La nota referenciada anteriormente es un ejemplo de tal situación.
-
Algunos hechos de importancia:
Al respecto, Juan Erviti, Doctor en farmacia y editor del Boletín farmacéutico de Navarra, España, mencionó unas apreciaciones importantes en el marco de la charla “Daños Potenciales asociados a las vacunas COVID-19” (6) en la que se hacen una serie de reflexiones y recomendaciones, de las cuales se destacan las siguientes a la luz de la seguridad de las vacunas:
- Hay Eventos Adversos graves asociados posiblemente a las vacunas COVID-19 que no se han documentado con la veracidad debida, algunos de estos se presentan en la siguiente tabla:
| Sistema | Posibles Eventos Adversos Graves |
| Cardiovascular | Miocarditis, Infarto agudo de miocardio, ictus, crisis hipertensivas. |
| Neurológico | Mielitis Transversa, síndrome de Guillaín-Barré (Leer: “Síndrome de Guillain-Barré y la vacuna de Janssen, ¿Debemos preocuparnos?”. |
| Inmune | Reacciones anafilácticas, enfermedad autoinmune, deterioro de la inmunidad natural. |
Tabla 1. Posibles eventos adversos graves asociados a Vacunas. Elaboración propia (6)
- Derivado de lo anterior, se deben realizar todos los ensayos clínicos con toda la rigurosidad del caso, muchos Eventos Adversos pueden ser identificados con un mayor número de pacientes y seguimientos prolongados en el tiempo. Erviti presentó casos donde en distintos ECA algunos EAPV no se reportaron de manera correcta, siendo enmascarados con otros eventos o por aparentes limitaciones editoriales a la hora de publicar.
- En ciertas investigaciones, los aspectos de seguridad no son de relevancia o se da prioridad a los desenlaces de eficacia en las publicaciones científicas, aspecto que se dificulta aún más por la corta duración de los ensayos.
- Es perentorio fortalecer los programas de FV, en especial aquellas actividades orientadas a la notificación espontánea de los EAPV, ya que en muchas ocasiones hay un subregistro de los eventos que realmente ocurren.
- Se hace un llamado a la transparencia en lo que respecta a datos de vacunas, incluyendo datos brutos de ensayos clínicos, estudios observaciones y Fase IV.
- No se pueden sugerir dosis adicionales de vacunas sin tener la evidencia suficiente sobre eficacia y seguridad. Al Respecto Misión Salud cuenta con una nota previa.
Bibliografía
- (1) 20 minutos. Dos años de la pandemia que nos cambió la vida. Nota de Prensa Disponible en: https://www.20minutos.es/especiales/especial-dos-anos-declaracion-pandemia-covid-oms/ Fecha de consulta: 10 de marzo de 2022
- (2) Troy D, Beringer P. Remington: The Science and Practice of Pharmacy. Lippincott Williams & Wilkins, editor. 2006.
- (3) Organización Panamericana de la Salud. Buenas Prácticas de Farmacovigilancia para las Américas Buenas Prácticas de Farmacovigilancia para las Américas. Washington. Washington, D. C; 2011.
- (4) World Health Organization. Uppsala Monitoring Centre. The importance of pharmacovigilance. Safety Monitoring of Medical Products. United Kingdom: WHO; 2002.
- (5) Ministerio de Salud y Protección Social. Boletín #9: Enero de 2022 Vigilancia de Eventos Adversos Posteriores a la Vacunación (EAPV) contra COVID-19 en Colombia Periodo del reporte: 17 de febrero de 2021 al 15 de enero de 2022. Disponible en: https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/VS/ED/boletin9-farmacovigilancia-vacunas-ene2022.pdf Fecha de consulta: 10 de marzo de 2022
- (6) Erviti, J. Daños Potenciales asociados a las vacunas COVID-19. Conferencia del 01 de marzo de 2022.
[1] Una RAM se define como “cualquier reacción nociva no intencionada que aparece a dosis normalmente usadas en el ser humano para profilaxis, diagnóstico o tratamiento o para modificar funciones fisiológicas”.
______________________________
El contenido de este artículo está bajo la responsabilidad exclusiva de su(s) respectivo(s)(as) autores(as), por lo que sus contenidos no comprometen a Misión Salud.






