Por Manuel Machado
Mensajes Clave
- El proceso de desarrollo de un nuevo medicamento o vacuna es complejo y extenso. Requiere de 10 a 16 años de investigación aproximadamente.
- Rusia registró una vacuna para COVID-19 sin estudios fase III, los cuales son necesarios para demostrar seguridad y eficacia.
- Hay riesgos potenciales si se aprueban medicamentos o vacunas de manera acelerada sin completar todos los ensayos clínicos con rigurosidad.
- Introducción
Con la aparición del SARS-CoV-2 los esfuerzos por encontrar un medicamento y/o vacuna son cada vez mayores, y han puesto a los países en una carrera contra el tiempo con tal de poner fin a esta pandemia que tantas dificultades ha traído a nivel de salud pública. No obstante, el proceso de desarrollo de un nuevo medicamento o vacuna que cumpla con esta misión no es sencillo. La investigación y producción de uno de éstos es bastante extensa y compleja. En promedio, el proceso puede durar entre 10 a 16 años y se realizan inversiones considerables de dinero antes de su aprobación y uso en las poblaciones.
Recordando rápidamente las etapas de desarrollo de un nuevo medicamento
Para dar un panorama muy general de cómo se desarrolla un medicamento describiremos el paso a paso global. El proceso inicia con estudios de pre-formulación y formulación, en los que se definen los ingredientes activos, excipientes y la tecnología involucrada, se revisan los procesos de escalado, estabilidad y establecimiento de los procesos de producción. Posteriormente se realizan estudios preclínicos en pequeños animales para evaluar efectos terapéuticos. Una vez concluidos éstos, se pasa a los estudios clínicos que constan de 4 fases (1):
| Estudios Fase I | Estudios Fase II | Estudios Fase III | Estudios Fase IV |
| Se realizan en una cantidad pequeña de personas voluntarias sanas, el objetivo es conocer si el medicamento es tolerado, efectos adversos, tolerancia, vía de administración y propiedades farmacocinéticas no detectadas en fases preclínicas anteriores. El número usual de participantes oscila de 20 a 100 (2-3) | En este caso el objetivo de los estudios es evaluar posibles dosis y eficacia (es decir, que el fármaco cure en condiciones controladas), se hacen las pruebas en pacientes que tengan la enfermedad de interés. Suelen emplearse en el orden de cientos de pacientes (1-3). | Los ensayos fase 3 son de los más importantes para demostrar si un fármaco funciona, En los estudios fase III se aporta más información de eficacia y seguridad que no se haya detectado en etapas previas, se hacen en mayor número de pacientes (orden de miles) y en varios lugares. Al finalizar estos estudios el nuevo medicamento o vacuna sale al mercado (1-3). | Con la autorización del Registro Sanitario el medicamento/vacuna se usa en condiciones reales y en todo tipo de pacientes. Los objetivos de estos estudios están enfocados en la seguridad del medicamento, es en este punto donde la autoridad sanitaria debe intensificar los programas de Farmacovigilancia para identificar nuevos efectos perjudiciales y clasificar mejor los efectos adversos/secundarios ya conocidos no observados en las fases anteriores, así como los efectos terapéuticos reales y posibles nuevos usos del medicamento. Si en esta etapa se descubre que el fármaco tiene más efectos perjudiciales que benéficos los estudios pueden ser suspendidos, situación que debe mantenerse a pesar de la emergencia sanitaria como la que se está viviendo (4). |
¿Qué está ocurriendo con las vacunas actuales para COVID-19?
Dada la situación de emergencia sanitaria causada por el COVID-19, la prioridad para los países es encontrar algún fármaco o vacuna que sea efectiva y segura, no obstante se le está pidiendo a la comunidad científica que logre un producto farmacéutico en dos años (o antes si fuera posible) cuando normalmente toma 10 a 16 años. De hecho, algunos países como Rusia habían registrado su vacuna antes de terminar la fase III de los ensayos clínicos en agosto de 2020.
Para ilustrar la situación presentamos la siguiente figura que compara el tiempo que toma desarrollar un nuevo medicamento/vacuna en condiciones normales con el que han tomado algunas de las vacunas para COVID-19 que se encuentran en proceso de desarrollo en el marco de la pandemia.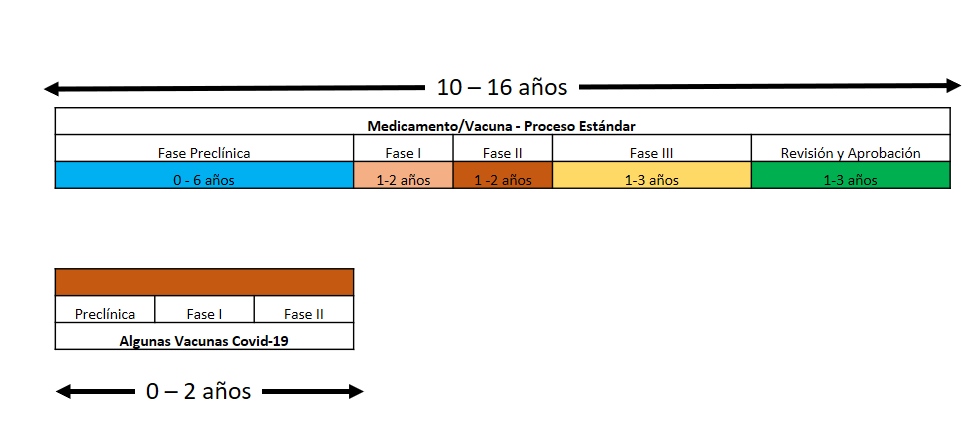
Figura 1: Comparación de tiempos de desarrollo de un medicamento/vacunas normales con algunas vacunas para COVID-19. Elaboración propia.
¿Qué implicaciones habría si se aprueban vacunas de manera acelerada?
El aprobar una vacuna de manera acelerada sin completar todos los estudios correspondientes podría traer graves consecuencias para las sociedades, entre las cuales destacamos (5):
- Riesgo de que se introduzca una vacuna que no se haya estudiado de manera adecuada y por ende, tenga fallas en eficacia que cumplan con el objetivo de inmunización, o en el peor de los casos genere efectos secundarios graves para las personas.
- Generación de falsas esperanzas en la población, lo que podría generar decepción en los individuos que decidieron aplicarse la vacuna en su momento y desconfianza a aplicarse otras vacunas a futuro.
- Riesgo de tomar malas decisiones para los países, en especial aquellos que están asegurando dosis de vacunas, ya que pueden comprar una vacuna que no funcione provocando pérdidas económicas graves con el correspondiente impacto social que esto implica para una nación.
- Los movimientos antivacunas no fundamentados en evidencia tendrían un argumento más para continuar desprestigiando a las mismas.
- Limitar el número de personas que se dejarían aplicar la vacuna y dificultar la continuación con los ensayos clínicos aleatorios.
En el marco del evento de Biosimilars LATAM 2020, exponentes del Centro de Pensamiento, Información y Poder presentaron una investigación realizada por Nicholas S. Downing y colaboradores donde se puede evidenciar algunas implicaciones de aprobar productos de manera acelerada. En dicha publicación se revisaron eventos de seguridad (efectos adversos) postcomercialización de medicamentos aprobados por FDA (autoridad sanitaria en los Estados Unidos) entre 2001 y 2010 y se muestra que hubo un mayor porcentaje de eventos de seguridad en los productos de aprobación acelerada en comparación con los de aprobación estándar evidenciando que productos acelerados podrían traer más riesgo de reacciones adversas, posiblemente por la disminución en tiempos de revisión y calidad de la evidencia (6).
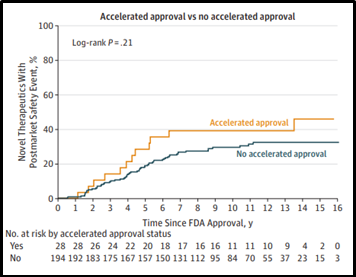
Figura 2: Porcentaje de eventos en seguridad en productos farmacéuticos aprobados normalmente Vs. Aprobación acelerada. Tomado de Downing et al (6).
Si bien las autoridades sanitarias deben garantizar y aprobar las vacunas lo más rápido posible, no hay que perder el horizonte científico ni el rigor metodológico, la aprobación del uso de emergencia de una vacuna debe realizarse con toda la seriedad del caso, aprobar vacunas con prisa puede ser más perjudicial que benéfico.
Del afán no queda sino el cansancio.
Bibliografía
- Jacqueline M. Investigación y desarrollo de nuevos medicamentos: de la molécula al fármaco. Rev méd Chile. 2001;9(1).
- Troy D, Beringer P. Remington: The Science and Practice of Pharmacy. Lippincott Williams & Wilkins, editor. 2006.
- Guerrero G. Las fases en el desarrollo de nuevos medicamentos. Rev Fac Med UNAM. 2009;5(6):260–4.
- Organización Panamericana de la Salud. Buenas Prácticas de Farmacovigilancia para las Américas Buenas Prácticas de Farmacovigilancia para las Américas. Washington. Washington, D. C; 2010. P 78.
- Paredes N. Vacuna contra la covid-19 | “Hará más mal que bien”: los peligros de aprobar una fórmula antes de que terminen los ensayos clínicos. Nota de Prensa. 4 de septiembre de 2020. Disponible en https://www.bbc.com/mundo/noticias-53986329?at_custom3=BBC+Mundo&at_medium=custom7&at_custom1=%5Bpost+type%5D&at_campaign=64&at_custom4=F9139A2E-F598-11EA-8EEB-2C984D484DA4&at_custom2=twitter
- Downing S. et al. Postmarket Safety Events Among Novel Therapeutics Approved by the US Food and Drug Administration Between 2001 and 2010. JAMA. 2017;317(18):1854-1863.






