Versión digital


 (Excepto Latinoamérica)
(Excepto Latinoamérica)
Versión física: En las principales librerías del país

La Política Farmacéutica Nacional 2012, las medidas de control de precios de los últimos años y el decreto 1782 de 2014, de regulación del registro sanitario de medicamentos biológicos, se resaltan y reciben como pasos que avanzan hacia una política sanitaria coherente al servicio del interés público. En entrevista del…
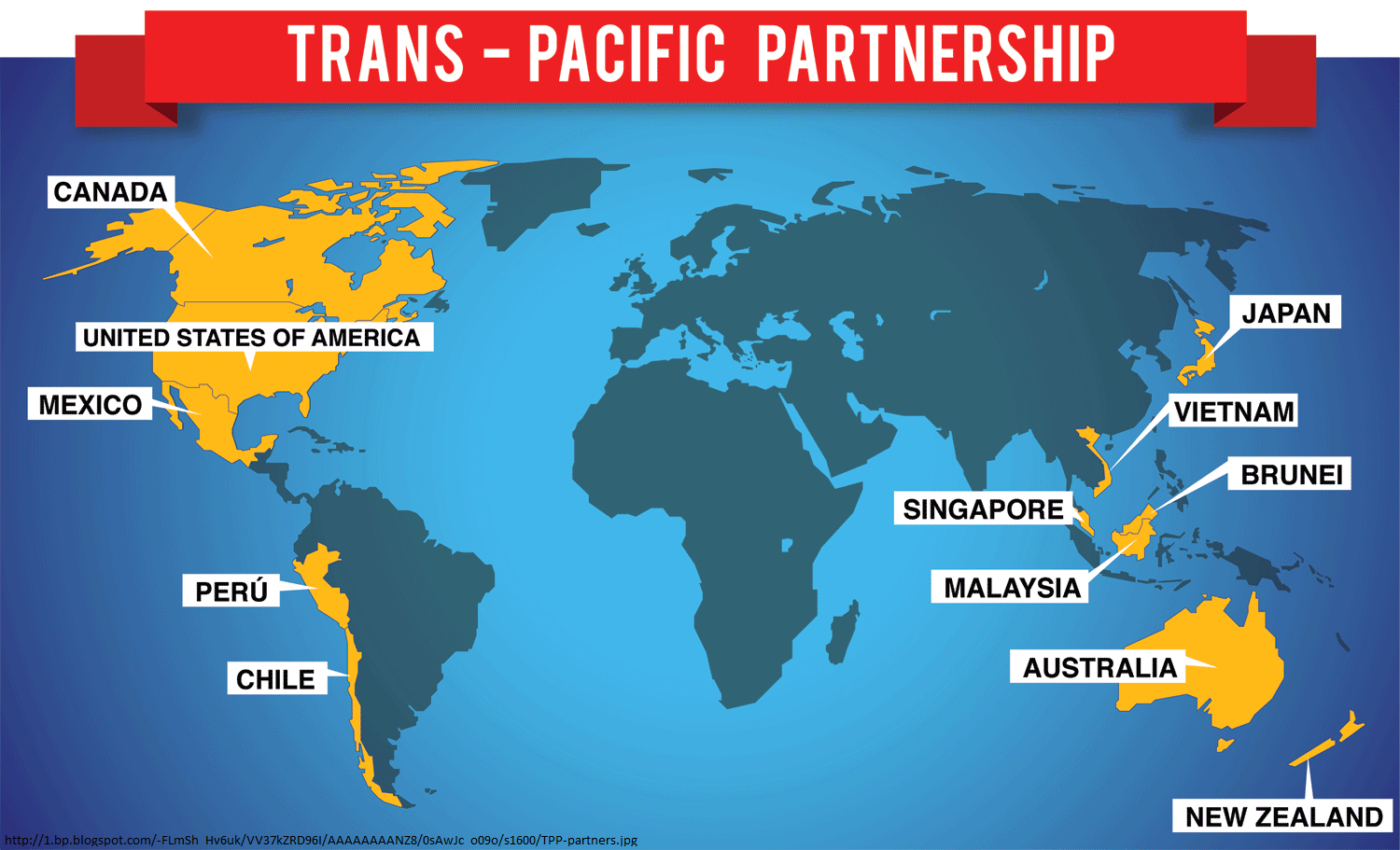
Misión Salud ha venido monitoreando la evolución del Acuerdo de Cooperación Económica trans-Pacífico, conocido como TPP. Aunque Colombia no hace parte de los firmantes iniciales de este acuerdo ha manifestado públicamente querer adherirse a él. Dado que los documentos que han surgido de las negociaciones de este acuerdo han sido…

Concluye el editorial: “En síntesis, la Política Farmacéutica Nacional va por buen camino, pero el balance definitivo se hará cuando los logros que hoy muestra se traduzcan de verdad en indicadores de bienestar y en la consolidación de una cultura de uso racional de los medicamentos. Lo alcanzado demuestra que…
“Existe pues un déficit de investigación clínica en Colombia, la cual debería convertirse en una prioridad, y ser no solo enseñada sino estimulada con reglas claras, precisas y permanentes. No en vano la investigación propia y original es considerada un motor de desarrollo. ¿Quién responde?” *Juan Manuel Anaya Fuente: Periódico…
En 2008, Ifarma (representante AIS en Colombia), Essential Action, Mesa de Organizaciones con Trabajo en VIH SIDA, Fundación Henry Ardila, RECOLVIH y Misión Salud, presentaron la primera solicitud de Licencia Obligatoria en Colombia adelantada por la sociedad civil. Descarga: 200806 Documento técnico
La Directora General de la OMS deberá convocar una reunión intergubernamental antes del 15 de octubre próximo, en la que se ha de discutir el borrador presentado en la pasada Asamblea Mundial (mayo). Este texto recibió diversas críticas por parte de representantes de ONGs sin fines de lucro.
Lea aquí la noticia completa
El documental realizado por la ONG Farmamundi explica por qué India se ha convertido en un líder mundial en la fabricación de medicamentos genéricos y sigue el proceso legal y social del llamado Caso Glivec, donde Novartis llevó al gobierno de la India a los Tribunales de Justicia por la patente de este medicamento contra el cáncer. Financia ACCD y Ajuntament de Barcelona.
Este es un fragmento extraído del documental.
Farmamundi: la farmacia del mundo from Misión Salud on Vimeo.
Para ver el documental completo hacer click aquí
Durante 2014 Misión Salud, como parte del CVCS, participó en el acompañamiento de la emisión del decreto que regula el otorgamiento de registro sanitario a medicamentos biológicos y biotecnológicos.
En este proceso el CVCS entregó a la comunidad en general un documento de caracter técnico-político “Medicamentos biotecnológicos sin barreras” para aportar a los tomadores de decisiones en particular y a la ciudadanía en general, con base en la información actual disponible y en los procesos que se han llevado hasta este momento desde los contextos científico, político, económico y social, elementos claves para facilitar el análisis del proyecto de reglamentación del Gobierno Nacional y despejar las dudas que puedan existir en cuanto a la idoneidad y pertinencia de una regulación que asegure al mismo tiempo calidad, competencia y acceso a los medicamentos biológicos y biotecnológicos, para beneficio de los pacientes y de la salud pública.
Superando enormes presiones políticas, el 18 de septiembre de 2014 fue firmado el decreto 1782, el cual regula el registro sanitario de medicamentos biológicos y biotecnológicos, garantizando la seguridad y eficacia de este tipo de medicinas y permitiendo a los pacientes disponer de alternativas terapéuticas de igual calidad y menor precio.
En cumplimiento de lo establecido en el artículo 22 del Decreto, el Gobierno ha de expedir las guías de inmunogenicidad, estabilidad, y de elaboración de planes de gestiones de riesgo para que el Decreto 1782/2014 entre en vigencia. Este proceso está actualmente en curso y su desenlace impactará favorable o desfavorablemente el acceso de las personas a estos medicamentos y, por ende, la sostenibilidad del sistema de salud actual.
A propósito del proceso en curso, el pasado viernes 29 de mayo la emisora de difusión nacional La W explica cómo el potencial impacto de este decreto en favor del acceso a medicamentos y la sostenibilidad del sistema de salud en Colombia y su posible replicación en otros países, sea una de las causas de la reestructuración de Afidro (Asociación de Laboratorios de investigación y Desarrollo). Escuchar programa.
El propósito del presente documento es aportar a los tomadores de decisiones en particular y a la ciudadanía en general, con base en la información actual disponible y en los procesos que se han llevado hasta este momento desde los contextos científico, político, económico y social, elementos claves para facilitar el análisis del proyecto de reglamentación del Gobierno Nacional y despejar las dudas que puedan existir en cuanto a la idoneidad y pertinencia de una regulación que asegure al mismo tiempo calidad, competencia y acceso a los medicamentos biológicos y biotecnológicos, para beneficio de los pacientes y de la salud pública.
Descarga el archivo original Medicamentos Biológicos sin Barreras